Rumus Laju Reaksi Kimia, Pengertian dan Contohnya
Rumusrumus.com Pada kesempatan kali ini kita akan membahas ilmu kimia tentang laju reaksi, memahami laju reaksi, rumus laju reaksi, pengaruh laju reaksi dan juga faktor laju reaksi
Memahami Laju Reaksi
Laju reaksi adalah tingkat penurunan ( reaktan/reagen ) atau tingkat kenaikan ( hasil/produk reaksi ). Laju reaksi ini menggambarkan seberapa cepat atau lambatnya suatu benda reaksi kimiasedangkan reaksi kimia adalah proses perubahan zat (reagen) menjadi zat baru dan disebut produk.
Contoh Reaksi Kimia
Beberapa reaksi kimia terjadi sangat cepat. Sodium yang dimasukkan ke dalam air akan menunjukkan reaksi yang sangat cepat, misalnya dengan kembang api Dan petasan yang tersulut. Bensin akan lebih cepat terbakar dibandingkan minyak tanah.
Namun, ada juga reaksi kimia yang berjalan lambat. misalnya: Proses besi berkarat, Memerlukan waktu yang lama sehingga laju reaksinya disebut lambat. Cepat atau lambatnya suatu reaksi kimia terjadi dinyatakan dengan laju reaksi.
Rumus Laju Reaksi
Laju reaksi kimia bukan hanya sekedar teori, tetapi dapat dirumuskan secara matematis
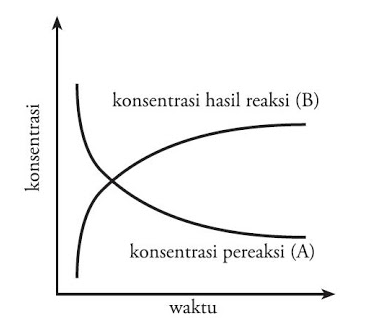
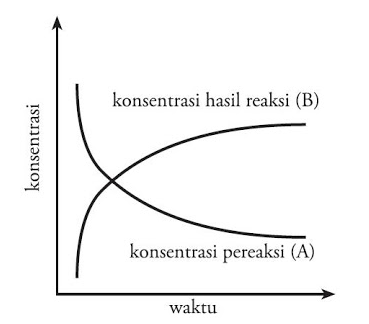
Pada reaksi kimia: A → B, laju perubahan zat A menjadi zat B ditentukan oleh banyaknya zat A yang bereaksi atau banyaknya zat B yang terbentuk per satuan waktu.
Jika reaktan A direduksi maka hasil reaksi B akan bertambah
Faktor-Faktor yang Mempengaruhi Laju Reaksi
Laju reaksi suatu reaksi kimia dapat dipengaruhi oleh beberapa faktor, misalnya luas permukaan zat yang bereaksi, konsentrasi reaktan, suhu terjadinya reaksi kimia, dan ada tidaknya katalis. Seiring dengan terjadinya proses reaksi kimia, ada satu hal yang harus dipelajari untuk mengetahui berlangsung atau tidaknya suatu reaksi kimia, yaitu tabrakan. Reaksi kimia dapat terjadi bila ada tabrakan antar molekul zat yang bereaksi. Tabrakan hanya tumbukan efektif yang menghasilkan reaksi kimia. Tumbukan yang efektif harus memenuhi dua syarat, yaitu posisi yang tepat dan energi yang cukup.
Pengaruh terhadap Laju Reaksi
Pengaruh konsentrasi terhadap laju reaksi
Jika konsentrasi suatu larutan semakin besar, maka larutan tersebut akan mengandung semakin banyak partikel sehingga partikel-partikel tersebut akan tersusun lebih rapat dibandingkan dengan larutan yang konsentrasinya lebih rendah. Susunan partikel yang padat memungkinkan terjadinya tumbukan yang lebih banyak dan kemungkinan terjadinya reaksi yang lebih besar. Semakin besar konsentrasi suatu zat maka semakin cepat laju reaksinya.
Pengaruh luas permukaan terhadap laju reaksi
Apabila reaktan tercampur maka akan terjadi tumbukan antar partikel reaktan pada permukaan zat. Laju reaksi dapat ditingkatkan dengan memperluas luas permukaan kontak dengan zat, yang dilakukan dengan memperkecil ukuran reaktan.
Pengaruh suhu terhadap laju reaksi
Partikel pada zat yang selalu bergerak. Jika suhu zat dinaikkan maka energi kinetik partikel akan meningkat, sehingga tumbukan antar partikel akan mempunyai energi yang cukup melebihi energi aktivasi. Hal seperti ini dapat menyebabkan lebih banyak tabrakan terjadig efektif
Pengaruh katalis terhadap laju reaksi
Laju reaksi yang lambat dapat dipercepat dengan menambahkan zat lain tanpa meningkatkan konsentrasi atau suhu reaksi. Zat ini disebut katalis. Katalisator mampu mempercepat laju reaksi, tetapi tidak mengalami perubahan kimia sehingga pada akhir reaksi zat tersebut dapat diperoleh kembali.
Baca Juga: